前言
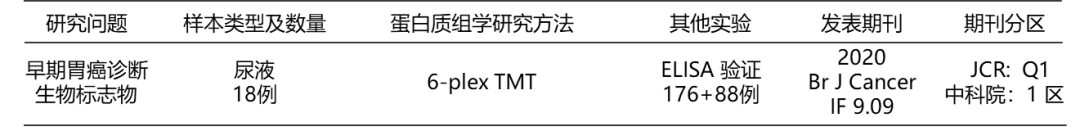
今天带来一篇2020年发表于British Journal Of Cancer(IF=9.09)的文章,标题为《新型尿蛋白生物标志物组用于胃癌早期诊断》。文章突出了蛋白质组学在病例对照研究的应用。
胃癌(Gastric Cancer, GC)起源于胃黏膜上皮,不仅是全球第五大常见恶性肿瘤,还是第三大致死癌症。按照国际TNM的分期标准,胃癌通常被分为四期(Ⅰ、Ⅱ、Ⅲ、Ⅳ),其中Ⅰ期胃癌5年生存率大于90%,而伴有远端转移的Ⅳ期胃癌5年生存率仅为15%。因此早期诊断对于胃癌的治愈至关重要,但早期胃癌无明显症状,少数人有恶心、呕吐或类似溃疡病的上消化道症状,难以发现和引起重视。
目前,内窥镜检查是诊断胃癌的金标准,但由于其高侵入性、风险性以及需要资金和时间成本,不适用于大规模筛查。幽门螺杆菌(Helicobacter pylori)引起的萎缩性胃炎是胃癌形成的主要原因之一,幽门螺杆菌抗体的血清学检测适用于萎缩性胃炎高危人群的胃癌筛查。但筛查幽门螺杆菌活动性感染不足以诊断胃癌,因为其假阳性率高,因此不建议以人群为基础进行幽门螺杆菌抗体的胃癌检测。总之,目前的各种临床检验方法,均难以便捷、有效的进行胃癌的早期诊断。
本文旨在寻找胃癌早期检测的非侵入性生物标志物,可用于大规模筛选,以提高胃癌的可治愈性。
实验设计:病例对照研究

作者通过三家日本研究机构收集从2012年9月到2017年6月,共有372例患者尿液,其中HC(Healthy Control)197例,GC患者175例。通过年龄及性别倾向性评分后,纳入282例患者(HC 138例、GC 144例)作为本研究的完整队列。随机分配后,以发现队列18例、训练队列176例、验证队列88例样本展开本次研究。首先在发现队列里通过6-plex TMT定量蛋白质组学筛选出7个候选标志物,结合作者前期研究ADAM12尿蛋白胃癌生物标志物以及H. pylori的病理特点,使用176例样本通过ELISA筛选出5个尿液候选生物标志物及对应的标志物组合。最后在88例样本队列中评估出效果最好的候选标志物组合,并且进一步以性别为界限,整体筛选出可区分HC和Ⅰ期胃癌患者的最优候选标志物组合。
本文发现uTFF1 + uADAM12 + H. pylori尿液生物标志物组合显著区分HC和GC患者;并且在性别特异性生物标志物的分析中,发现uTFF1 + uADAM12 + H. pylori组合适用于对男性GC诊断,而uTFF1 + uBARD1 + H. pylori 组合适用于女性GC诊断;以上两种诊断组合同样可区分相对应的Ⅰ期GC患者和HC。本文筛选出的新型尿蛋白生物标志物组合,可对早期胃癌人群进行非入侵性地精确诊断,提高胃癌可治愈性。
结果一:蛋白组学分析尿蛋白生物标志物
对发现队列18例尿液样本按照胃癌分期、性别、年龄及尿液总蛋白量进行匹配分析,将其分为6组,每组3个人的尿液蛋白合并收集后,使用6-plex TMT 标记定量方法进行分析。总共鉴定到1148个定量蛋白,并按照(1)蛋白质分子量较小(2)在胃中特异性表达的癌症/睾丸抗原或蛋白,这两个标准,最终筛选出7种尿液候选蛋白(TFF1, PGA3, BARD1, CCDC38, TINAGL1, NDRG1和DDX55)。作者前期研究发现ADAM12可作为诊断GC的良好尿蛋白生物标志物,在以下研究中,将其并入一起分析。
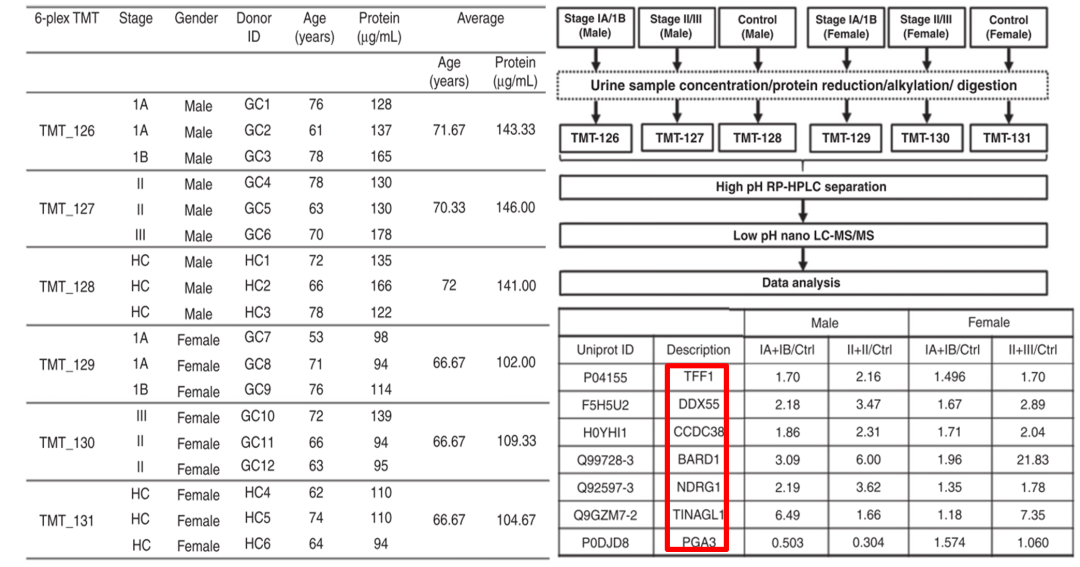
结果二:生物标志物的建立与验证
首先对研究队列中的HC和GC组的基线特征进行分析,由Table1可知,在训练队列和验证队列中,HC和GC组的年龄、性别或血清肌酐等均无显著差异,但GC组的H. pylori阳性率显著高于HC组(P < 0.001)。因此后续需将H. pylori纳入队列研究。
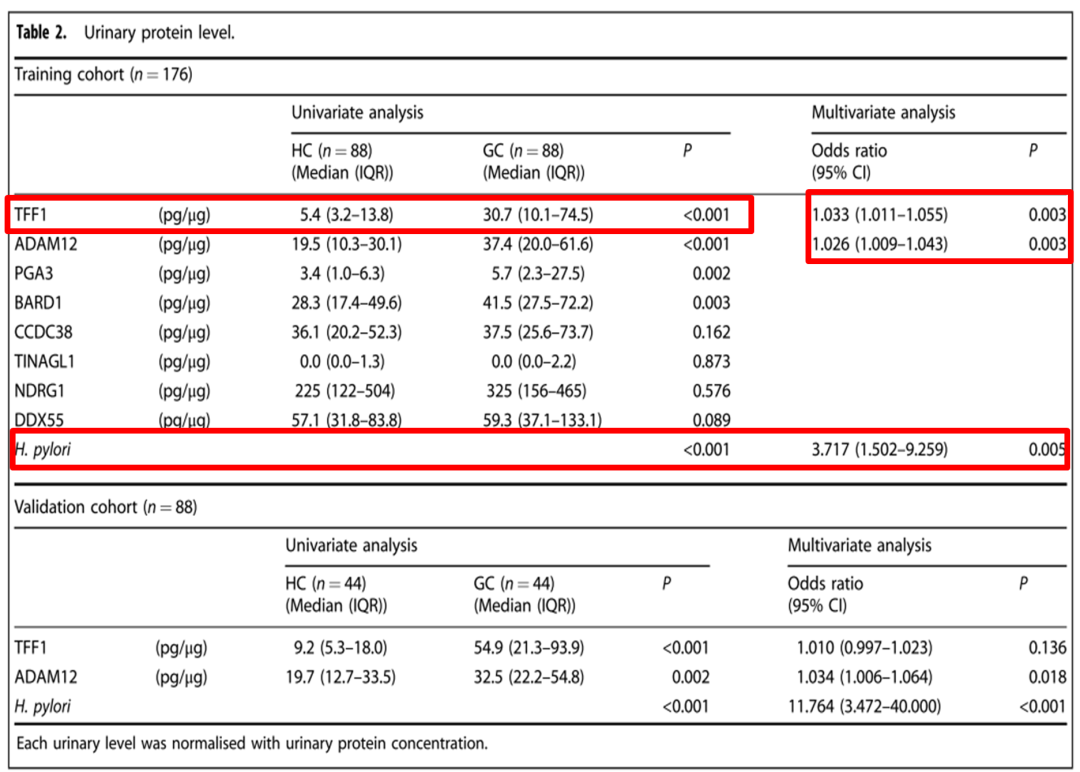
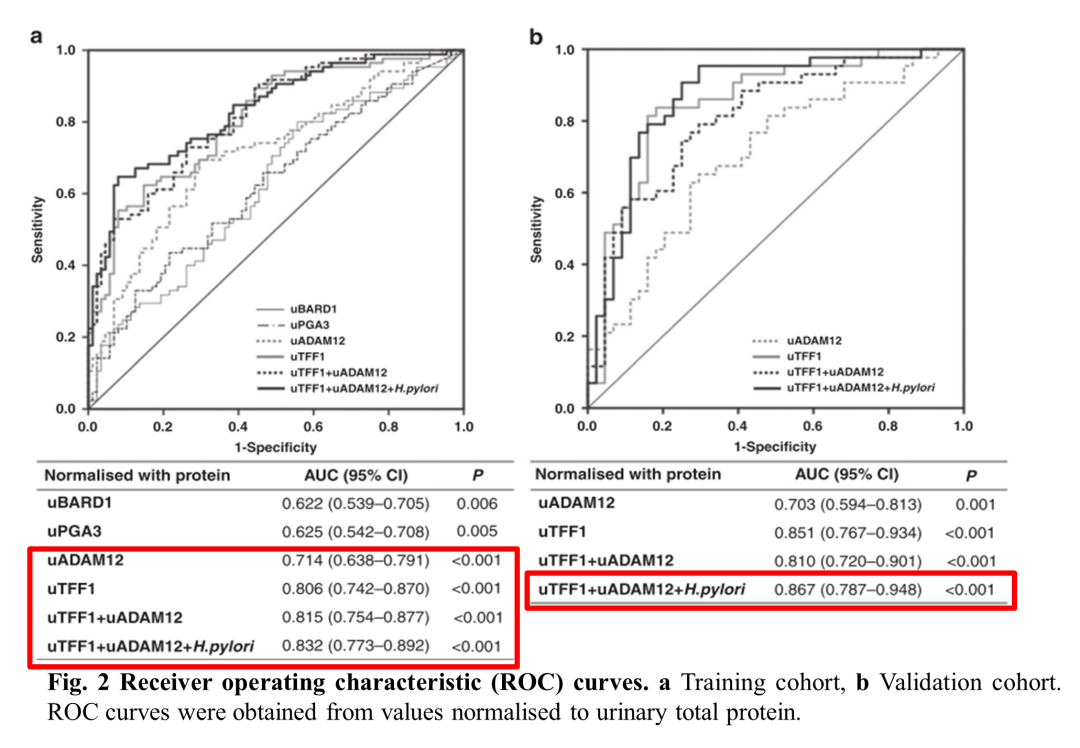
通过ELISA分析训练队列中8种候选尿蛋白水平,由Table2单因素分析显示,TFF1 (uTFF1)、ADAM12 (uADAM12)、PGA3 (uPGA3)和BARD1 (uBARD1)在GC组的尿蛋白水平显著高于HC组;多因素分析显示,uTFF1、uADAM12及H. pylori阳性率的差异作为胃癌诊断的特异性生物标志物均具有统计学意义,但uPGA3和uBARD1的差异均无统计学意义。因此,uTFF1、uADAM12和H. pylori阳性可作为胃癌的临时诊断生物标志物。此外,uTFF1、uADAM12、uPGA3和uBARD1在训练队列的受试者工作特征曲线(ROC)分析显示, uTFF1、uADAM12和H. pylori联合检测时,这些联合生物标志物在HC和GC之间的差异具有统计学意义(AUC= 0.832, 95% CI, 0.773 ~ 0.892)( Fig. 2a)。这些结果表明, uTFF1/ uADAM12/H. pylori组合可能是一个良好胃癌诊断的尿液生物标志物。
接下来,在验证队列中检验已建立的生物标志物组合的诊断质量。如Table2所示,在验证队列中,uTFF1、uADAM12和H. pylori在GC组中显著高于HC组。uTFF1+uADAM12+H. pylori的生物标志物组合显示AUC值为0.867 (95% CI, 0.787 ~ 0.948),进一步验证训练队列结果 (Fig. 2b)。以上结果表明uTFF1/ uADAM12/H. pylori可作为一个良好的胃癌诊断生物标志物组合。
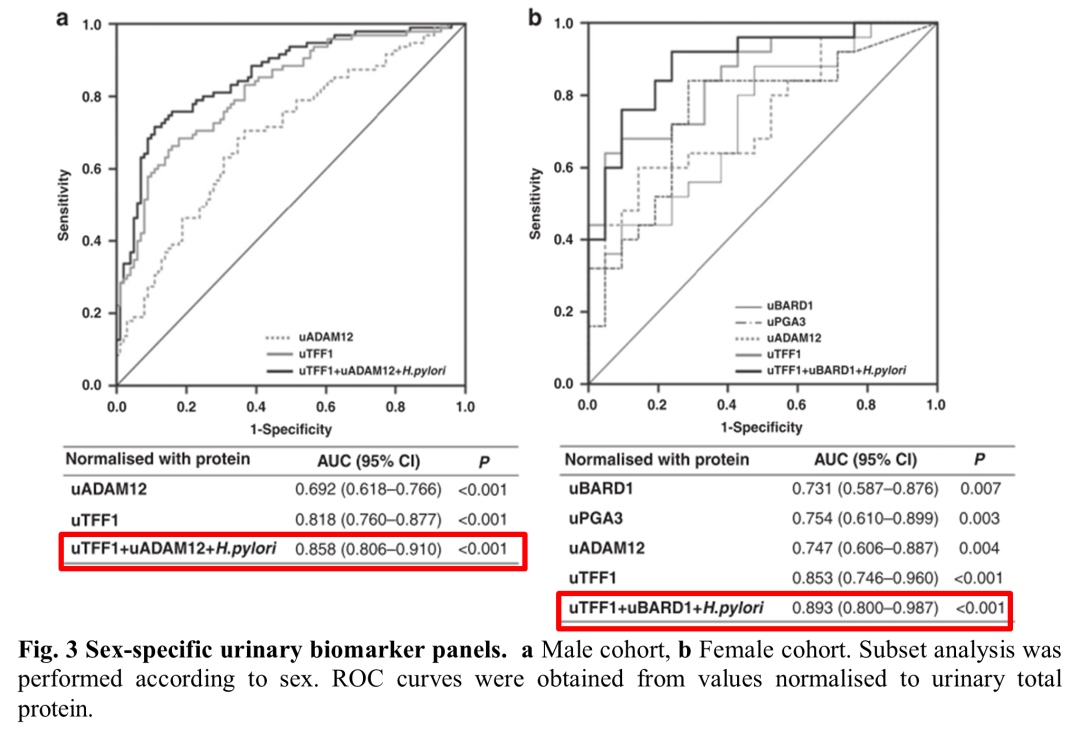
结果三:性别特异性的早期胃癌生物标志物鉴定
由于男女胃癌发病率达2:1,所以为了鉴别性别特异性的尿蛋白生物标志物,本文根据性别进行亚群分析。在男性队列中,uTFF1、uADAM12和H. pylori的尿液生物标志物组合显著区分了HC和GC组,其AUC值为0.858 (95% CI 0.806-0.910)( Fig. 3a);对于女性队列,由uTFF1、uBARD1和H. pylori尿液生物标志物组合也显示出良好的区分效果,AUC值为0.893 (95% CI 0.800 ~ 0.987)(Fig. 3b)。
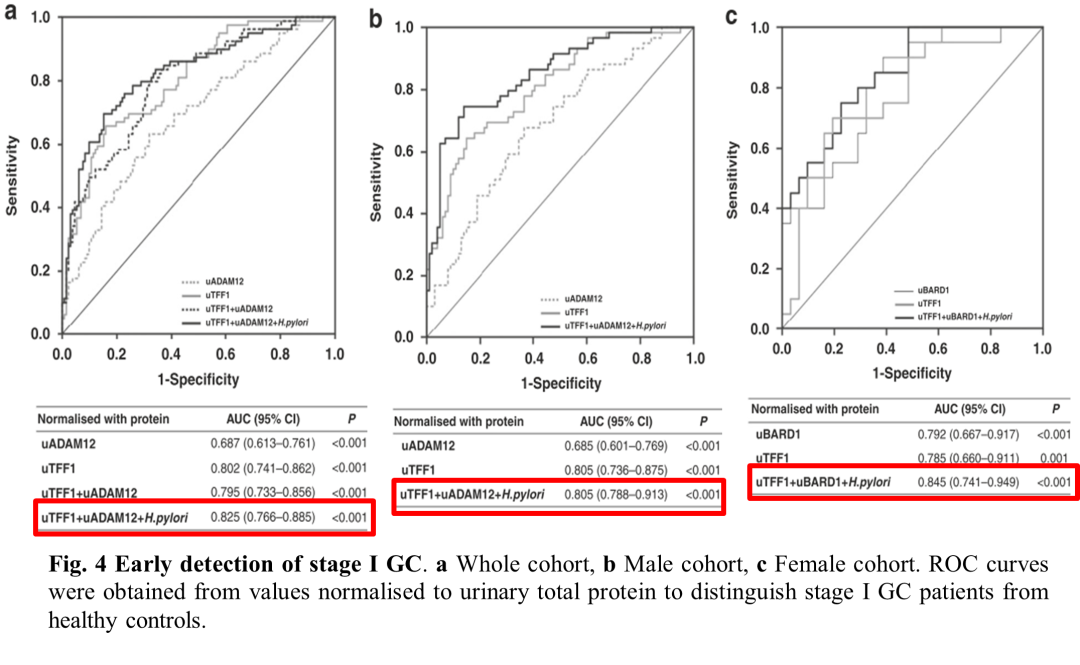
为了对胃癌早期患者进行进一步诊断,分析了HC和Ⅰ期胃癌患者样本。结果显示uTFF1、uADAM12和H. pylori的生物标志物组合可以区分HC和Ⅰ期胃癌患者,其AUC为0.825 (95% CI 0.766-0.885) (Fig. 4a)。此外,男性GC患者尿蛋白生物标志物组合uTFF1/uADAM12/H.pylori和女性GC 患者uTFF1/uBARD1/ H. pylori组合可分别诊断出男性和女性的Ⅰ期胃癌患者,其AUC值分别为0.805和0.845、特异性分别为91.5%和100%(Fig. 4b, c)。
结论
本文采用282例尿液样本展开回顾性的病例对照研究,首先在18例发现队列进行6-plex TMT标记蛋白定量,筛选出7个尿蛋白的候选胃癌生物标志物,之后通过176例训练队列样本和88例验证队列样本最终确定uTFF1/uADAM12/H. pylori和uTFF1/uBARD1/H. pylori尿蛋白生物标志物组合,可分别诊断男性和女性的Ⅰ期胃癌患者。
总结
本文是一篇结合病例对照研究设计和蛋白质组学分析的文章,采用较大样本量进行训练和验证,最终确定胃癌早期检测的非侵入性生物标志物组合,对于提高胃癌的可治愈性有一定临床意义。但本研究在蛋白组学的分析上还可以进一步完善,例如对差异蛋白进行必要的生物信息学分析,以提示相关疾病的发病机制;优化差异蛋白筛选条件,提高诊断标志物的精准度等。
TMT标记定量是一种经典的蛋白质组学定量研究策略,能够对复杂的生物样品进行深度定量检测,但由于其标记试剂的高成本和标记通量的限制,在大队列的临床研究中,针对尿液、血浆、唾液等成分较简单的临床样本进行定量检测时,使用DIA等无需标记的蛋白质组学定量方法往往能获得更好的效果。本研究中可能也是受限于TMT标记定量方法的限制,在发现队列中仅纳入18例样品,并且每3例混合后进行检测。由于临床样本的个体差异,队列过小可能导致筛选出的假阳性结果增多,并且也可能遗漏一些有效的标志物分子。
之前曾介绍过,结合多个蛋白分子标志物指标联合建模,并引入临床指标,能够有效提高诊断预测模型的区分性能。本研究也展示了应用2种临床指标与分子标志物联合建模的方式:1)临床指标可作为模型分层指标,如本研究中的性别指标,根据该临床指标分层后分别建立诊断预测模型;2)将临床指标纳入联合模型,如本研究中的H. pylori指标,与蛋白标志物分子合并建模,作为疾病的诊断指标。