今天小谱将给大家分享一个文章撰写指南,帮助大家写出一篇符合标准的临床蛋白质组学研究论文。本文来源于MCP期刊,标题为“Guidelines for Preparing Manuscripts Describing Research in Clinical Proteomics”(链接:https://www.mcponline.org/clinical)。这篇文章可以很好地帮助作者降低论文撰写的难度,在论文撰写过程不要遗漏必要信息。在此我们将这篇文章进行了完整翻译分享,并附上蓝色标注的小谱独家秘籍。下面开始进入正题吧!
阅前提示
指南的目的是提供足够的信息,供审阅者/读者能够评估、解释、比较和重现报告中的研究结果。其中包含强制性信息(星号*标记)和推荐性信息。作者在提交手稿时,还必须审查所对应期刊网站上需要完成的清单文件,这一点非常重要。
01
伦理批件
*需要提供一份由伦理机构/动物委员会(IRB/ACUC)批准将人类/动物生物材料用于本研究报告的研究目的的声明,包括知情同意书的详细信息(如适用),用于临床或生物标志物试验参与和/或原代细胞系开发。此外,应说明用于保护人类受试者的隐私的方法,如生物样本的识别/去识别和编码程序。
图1 中国临床试验注册中心网页
02
研究目标和设计
应提供研究设计的全面描述,包括研究的总体目标,特别注意以下要求:
-
*研究的阶段,例如发现、验证或确认阶段,并明确说明生物标志物、靶标、分析物所处的具体阶段,例如处于探索/发现阶段;临床前验证阶段等等。
-
*研究中受试者/样本的变化情况,包括初始病例数、每个分析阶段所包含的样本数量(对于更复杂/更大的研究,建议使用流程图表)以及受试者退出的原因。
-
在定义“鉴别诊断疾病特异性”生物标志物时,应将与感兴趣疾病的其他相似疾病的样本作为对照。
-
样本采集和/或研究执行的时间段。
-
用于计算样本量的α,β等统计学指标。
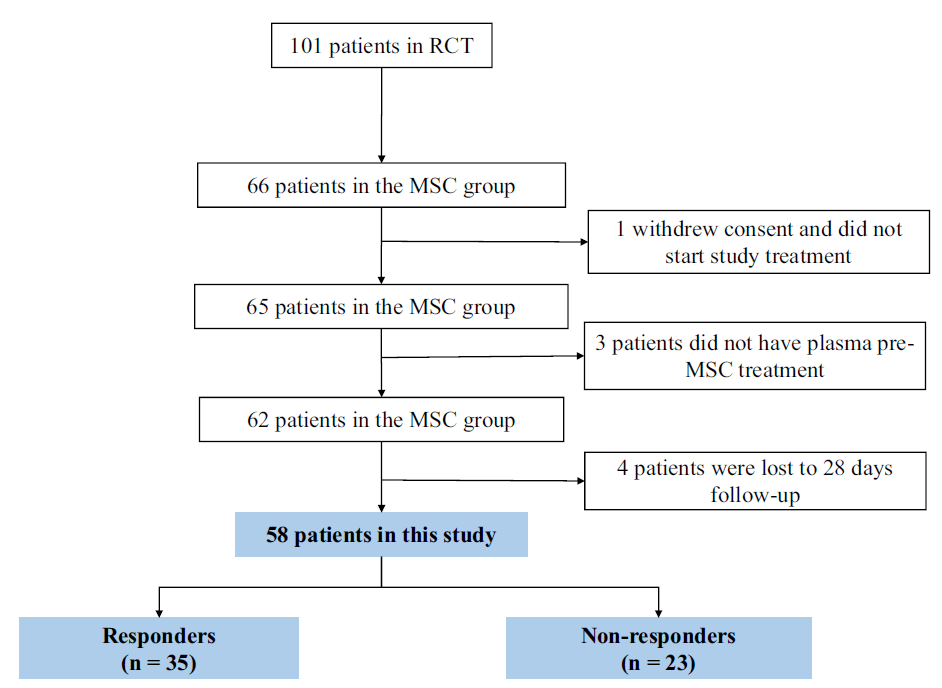
图2 人群纳入流程图
图片来源请见参考文献[1]
03
受试者来源与描述
-
*应描述受试者(或从中获得的材料)的来源和分类,至少包括以下几个方面的信息:
-
是前瞻性研究还是回顾性研究。
-
如何进行分层的。
-
是否进行样本匹配(年龄,性别等因素)。
-
是否将受试者进行随机化分配,如治疗、干预等。
-
*描述生物样本的来源(例如集中式生物库、内部生物库、临床试验收集、手术等)。
-
*提供队列的纳入/排除标准。
-
*对于所有采集样本的患者,需要对疾病或病症(包括已知的治疗方法)进行定义,并应包括:
-
疾病描述,如亚型、分期、分级、组织学和临床评分(如适用),以及这些是如何确定的。
-
使用标准医学术语(包括已知的ICD代码)的疾病类型,例如青少年糖尿病与非胰岛素依赖型糖尿病。
-
与采样时间相关的任何已知的潜在混杂因素,如术中或术前状态、服用的药物/麻醉剂等。
-
应提供研究和参考(对照)受试者的内在因素、人口统计学和临床特征,包括年龄、性别、疾病阶段和合并症等。
-
应描述试验治疗或其他干预措施。
-
应列出可能影响结果的外在因素、干预措施和生活方式因素,如吸烟史等。
-
如果合适,应提供随访的持续时间,包括中位数和范围。
04
生物样本质量
4.1组织样本
-
如果适用,应提供以下信息:
-
组织采集和处理的平均时间,以及时间范围。
-
*样本预处理的方法,例如福尔马林、乙醇、包埋介质、冷冻方法、裂解溶液等。
-
样本平均储存温度以及储存时间的平均值和范围。
-
*冷冻组织的固定和切割处理方式。
-
*若适用,生物样本相关成分的富集方法(如显微解剖、分馏)。
-
任何有关生物样本运送至中央储存库的资料,例如运输时间、温度条件等。
-
*报告实验中使用的生物样本的任何组织学检查。
-
如果对组织样本进行了免疫组织化学染色或其他检测,应说明病理审查是否是盲审,以及参与审查的病理学家们是否对结果达成了一致意见。
-
注意:审稿人和/或编辑可能会要求提供组织学证据(数字化或原始切片)。
4.2 体液样本
-
*对于血液和生物体液样本,应参考已发布的标准操作程序;如果没有,则应提供以下信息:
-
*收集的方法(如果是尿液样本,应说明采集方式:24小时收集、早晨首次、早晨第二次或随机尿液早期流或中段流。)。
-
*用于收集和储存的试管类型和大小。
-
*使用的添加剂,如抗凝剂、防腐剂和蛋白酶抑制剂(如果使用的话)。
-
处理条件,包括收集和分离之间的时间间隔、*离心条件、处理温度、处理和冷冻之间的时间间隙。
-
*储存温度和储存时长。
-
*冻融循环次数。
-
生物样本集在收集和处理过程中的任何变化。
4.3 原代细胞系
-
*对于原代细胞系的产生和使用,应提供以下信息:
-
有关受试者的原始生物标本的临床细节。
-
细胞系产生和鉴定的条件/方案,包括传代次数和分析的克隆数量。
4.4 统计考虑因素
-
*应详细说明统计分析策略,其中应包括:
-
正在检验的假设。
-
模型构建和验证。
-
所用统计算法的明确定义。
-
用于选择截止阈值和其他模型参数的理由。
-
探索性(训练)和验证性(测试)分析的独立性。
-
应提供有关统计分析的下列详细资料:
-
特征选择和多重假设检验策略。
-
测试的候选物(如标记物、靶标、分析物)的数量。
-
任何亚组进行分析的详细信息。
-
任何缺失的值以及如何处理这些缺失值。
-
*统计学估计p 值和/或置信区间。
-
在统计报告中,应包括对混杂因素的讨论以及为尽量减少其影响而采用的方法。
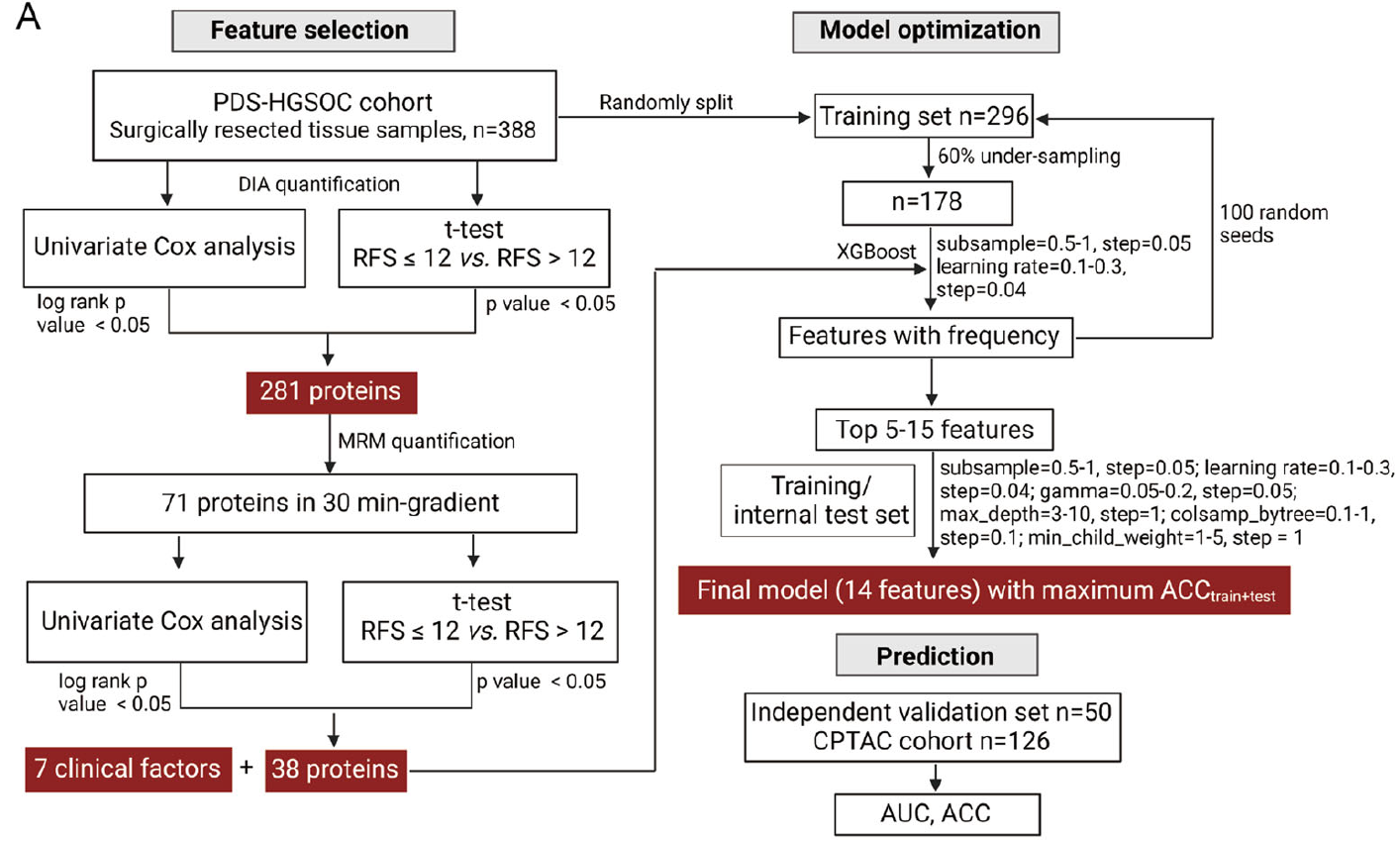
图3 建模流程图
图片来源请见参考文献[2]
4.5 技术考虑因素
-
*应描述所用分析过程/测定(如质谱、蛋白质、抗体、核酸阵列、免疫化学、二维凝胶电泳或其他测量技术)的性能特征(技术和过程,包括分馏、消化等)。对于技术和处理步骤(分馏、消化等),应描述噪声评估、再现性、归一化(例如阵列到阵列和蛋白质到蛋白质)、测量变化、特异性、检测限和定量信息。
-
期刊鼓励作者将原始数据存储在易于访问的数据库中,并提供该数据库的超链接,用于处理临床蛋白质组学文章收集的信息。期刊还强烈鼓励作者尽可能定义生物标志物,特别是用于验证研究的标志物。
-
应描述研究中所采用的质量控制和质量保证方法,包括如何进行样品分析,例如重复数、是否随机化等。
-
应描述任何用于模型构建、通路分析或数据可视化的任何软件包和生物信息学的工具。期刊政策要求所有使用的软件都向公众开放。
-
鼓励作者将原始数据放在可公开访问的数据库存储站点中。期刊将提供此数据库的超链接。
-
如果适用或已知,无论之前研究的性质如何,都应列出使用相同或部分样本的任何其他研究(最好通过文献参考)。
以上就是文章的全部内容。不难发现,随着临床蛋白质组学研究的深入,对其相关论文要求也是越来越高了,不管是从临床研究设计方案的合理性、样本检测的专业性、和数据分析的准确性都对研究者有较高的要求。想要快速进入蛋白组学研究中,需要优秀的临床蛋白质组学服务平台和专业团队。
谱度众合(武汉)生命科技有限公司目前已服务客户5000余名,遍布全国100余家研究型三甲医院,公司开发的临床蛋白组学解决方案致力于为客户提供更省心的服务、更稳定可靠的数据结果、更丰富详实的分析内容、满足更多元个性的研究方向。依托谱度众合人才团队建成的“生物标志物发现与药物靶点筛选平台”,经过10余年发展,在2023年被政府认定为“国家生物产业基地公共服务平台”以及“武汉市科技成果转化中试平台”,是华中地区最好的临床蛋白质组学平台。围绕该平台已成功布局专利技术50余项、发表SCI论文100余篇、获批国家及省市基金10余项。
我们将持续分享关于临床蛋白质组学论文撰写的相关经验,希望能帮您更高效地开展临床科研,用我们多年经验积累为您保驾护航。如果您对分享内容感兴趣的话,还请关注我们。
参考文献:
[1] Li TT, Yao WQ, Dong HB, et al. Plasma proteomics-based biomarkers for predicting response to mesenchymal stem cell therapy in severe COVID-19. Stem Cell Res Ther. 2023;14(1):350. Published 2023 Dec 10. doi:10.1186/s13287-023-03573-4
[2]Qian L, Zhu J, Xue Z, et al. Proteomic landscape of epithelial ovarian cancer. Nat Commun. 2024;15(1):6462. Published 2024 Jul 31. doi:10.1038/s41467-024-50786-z