研究方案如何选择?
伦理审核怎么做?
临床数据如何整理分析?
看这个系列就对了!
随着我国临床医学的发展,对我们医生朋友提出了更高的要求,临床要强,科研也要强。当晋升的独木桥越走越拥挤,当科研填满了诊疗工作之外的空隙,我们更应该用高效的方法,做有价值的科研,事半功倍!我们希望通过本系列文章,帮助您全面了解临床科研的标准流程,并提供切实可行的解决方案,让您的科研工作轻松顺利!
以临床蛋白质组学研究为例,开展临床科研工作有五大步骤:提出明确的临床问题 → 清晰的研究设计 → 伦理审核与临床研究注册 → 样本的采集与数据分析解释 →证据力度的思辨与成果产出(联系我们,这里的每一步小谱都可以提供帮助哦~)。作为本系列的第一期,小谱将借助一篇我司合作发表的文章,通过具体案例为大家简单梳理一下临床科研的开展流程,后续文章还会针对每一个步骤进行详细介绍,强烈建议大家收藏!
这个研究项目是希望建立一个临床模型,预测体外循环术后是否发生急性呼吸窘迫综合征(ARDS),文章于2023年发表在期刊Int J Surg(IF15.1)上。
第一步——明确的临床问题:从临床需求出发确定选题,关注临床意义
体外循环术(cardiopulmonary bypass, CPB)后易发急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS),ARDS的预后差,且尚无有效的治疗方法。因此,预测患者术后是否发生ARDS就是一个很好的切入点,有明确的临床意义。由此我们确定了研究目标——通过临床蛋白质组学相关技术,构建CPB-ARDS的风险预测模型,期望能够对CPB-ARDS的高风险人群进行预测,以便于及早采取合适的预防措施。
明确了研究目标,我们就可以按照PICO原则来确定选题,(P,研究人群participants;I,干预或暴露因素intervention or exposure;C,对照control;O,结局outcome)。该文章的研究对象为行CPB手术的病人;暴露因素为可能影响CPB术后发生/不发生ARDS的病患特征(可以是病人的一般情况、实验室检测指标、手术相关变量等常规临床变量,也可以是病人的蛋白质水平——生物标志物);对照为CPB术后未发生ARDS的病人;结局为CPB术后是否发生ARDS。
第二步——清晰的研究设计:紧扣研究目的,明确具体操作
在做研究设计时,有很多因素需要考虑,例如:慎重选项样本类型和取样时间点,明确纳排标准和结局指标,确保符合伦理,采用合适的统计分析方法……我司有专业的流行病学专家团队,能够为该部分研究的设计提供技术支持。
以这个研究为例,在设计时我们就考虑到了很多方面,其中比较重要的内容有:①CPB手术是发生ARDS的诱因,本研究设置了麻醉前、术后即刻、术后24h的3个采样点,分别分析不同时刻样本特征对结局预测效果,并相互比较取最佳。;②在做心脏手术的过程中血液样本比较容易收集,且血液中的生物标志物对预测心脏手术患者的预后有较高的应用价值,因此该研究采用血浆样本;③采样过程为手术中的固有步骤,并不算对研究对象施加额外干预,所以该研究为前瞻性的观察性研究——巢式病例对照研究;④为了控制混杂偏倚,该研究严格设定了研究对象的纳入排除标准;⑤由于CPB术后发生ARDS的时间一般在3天内,所以是否在术后3天内发生ARDS为本研究的主要结局;⑥研究结局的质控:ARDS诊断标准来自Berlin定义,与疾病开始时间、胸部X线平片或CT扫描、肺水肿及缺氧程度等多方面有关,为了保证ARDS诊断结果的权威性和可信度,将由2名专业医生独立做出诊断;⑦为增强预测模型的可信度,采用3个独立队列分别用于发现蛋白质生物标志物(biomarker)、验证biomarker并建立预测模型、以及验证预测模型。最终,该文章确定了如图2所示的技术路线图,共纳入3个独立队列和1个动物模型,研究者从血浆样本中找到了CPB术后发生ARDS的生物标志物,并联合蛋白质和临床变量构建了模型对ARDS的发生概率进行预测。
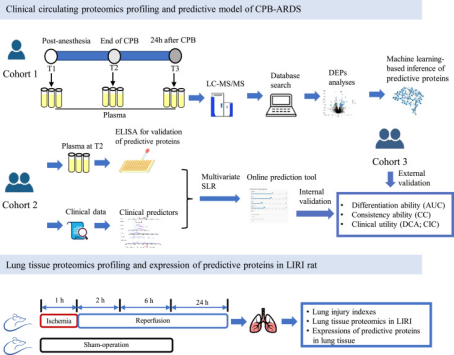
图2 技术路线图
看到这里,大家是否能够根据自己关注的临床问题,模仿这个案例拟定一个临床科研选题,并设计一套可行的研究方案呢?如果还是觉得有难度,别担心,联系我们,我们来协助您!
第三步——伦理审核与临床研究注册
根据2016年12月1日起开始实施的《涉及人的生物医学研究伦理审查办法》第二条所写:“该办法适用于各级各类医疗卫生机构开展涉及人的生物医学研究伦理审查工作”。所以只要研究涉及“人”,不论研究属于前瞻性、回顾性、观察性、干预性中的哪种类型,都需要进行伦理审查。这篇前瞻性的观察性研究通过了武汉协和医院机构审查委员会批准(批准号20200518),并在clinicaltrials.gov上进行注册(注册号NCTO4696172),动物实验也完全符合同济医学院实验动物中心的动物实验规范(IAUC编号2916)。
图3 伦理审查办法
第四步——样本的采集与数据分析解释:原始数据库+CRF表+结构化数据库+组学检测与分析
原始数据库:经过文献调研和专业经验,收集会影响术后发生ARDS的所有临床危险因素:①人口学资料和术前并发症;②术前实验室检查指标;③手术相关变量;④输血量。此外,还需收集诊断术后是否发生ARDS的依据:胸片、血气、超声心动图、临床症状等。以上资料和收集该资料的手段(采集操作以及检测仪器,服用药物、注射试剂的厂家和型号等)共同构成了原始数据库。
病例报告表(case report form,CRF):CRF表主要包括封面页、纳入排除标准的符合情况、基线资料、诊疗资料、随访资料等。针对临床项目最关心的临床诊疗资料,我们首推公认的量表、金标准或专家共识,比如:蒙特利尔认知评估量表、焦虑/抑郁自评量表、呼吸困难分级量表、日常生活能力量表等。CRF表既可以是纸质版,也可以是电子版。
结构化数据库:CRF表肯定是不适合直接用来做统计分析的,所以需要将其转化为结构化数据库。结构化数据是将所有信息进行系统的整理和展示的结果,很适合用来进行数据分析。这里我们推荐一款免费的工具——Epidata,既能录入纸质版CRF表信息、又能储存数据、还能直接导出为表格的工具。Epidata小巧且操作简单,甚至可以对双人录入数据进行核查,保证录入数据的真实可靠!如果大家感兴趣,本系列的后续文章中会介绍该软件的使用操作,大家记得关注我们并收藏本文哦。
组学检测与分析:前文提到的血浆样本邮寄至我司后,经过样品制备、质谱检测以及搜库流程,最终获得了一份定量蛋白数据表格,再联合由医生收集的临床数据表格,共同进行统计分析——产生了文章中人群描述、差异分析和建模评价相关结果图。人群描述主要是对研究对象的特征进行描述,说明研究结果的适用人群范围;差异分析是为了找到组间具有差异的临床变量和蛋白,这些差异变量可能具有临床意义;建模评价是建立预测不同临床结局的模型,并对模型的预测效果进行评价,择优选择。如果您对建模评价感兴趣,一定要看看我们的《生信分析 | 临床数据建模系列》。
第五步——证据力度的思辨与成果产出
如果大家看过很多高分文章会发现,高质量的临床研究需要通过多种模型和多种技术从不同角度来验证研究结果,一方面保证结果的准确性和可重复性,另一方面保证结果的外推性和应用价值。在这个研究中,我们从三个角度验证了结果:一是我们使用了动物模型中对关键蛋白进行了验证;二是我们在多个队列中验证了模型,使得结论具有外推性;三是使用了不同原理的定量技术——ELISA进行验证,这是一种可以进行绝对定量检测方法,利于后期将成果转化应用于真实的疾病诊断和预后场景。这些都属于证据力度思辨的过程,是衡量研究质量的关键。
最后,将研究结果按照一定的逻辑整理成图片和文字,突出研究的创新点和临床价值,就可以投稿发表啦!值得一提的是,我们的产品报告是借鉴了众多高分期刊的结果展示形式和图片配色,可以直接用于论文发表,还可以提供方法的英文文案,用起来非常省心省力哦!

谱度众合疾病诊断研究产品报告部分结果
以上就是临床科研步骤介绍啦~临床世界有许多隐藏的科研宝藏,临床医生作为离宝藏最近的人,是最有可能发现线索并挖掘宝藏的人!不过多数临床医生一方面临床工作非常忙碌,另一方面没有科研团队,科研上只能单打独斗,导致心有余而力不足。小谱拥有一支专业临床科研技术团队,拥有大量项目经验,应用先进的高通量质谱设备,从选题和设计开始,辅助医生和老师们高效轻松做科研~~~我们结合多年宝贵经验,不断推出多种细分场景的科研服务(疾病诊断研究蛋白质组学服务、疾病预后研究蛋白质组学服务、随机对照临床试验蛋白质组学服务、FFPE临床蛋白组学解决方案),联系我们了解更多哦~
在本系列后续文章中,我们将具体讲解临床方案设计、伦理审核和临床数据整理与分析三个环节的开展流程以及预期收获,联系我们,小谱还会提供一些模板材料供大家参考哦!欢迎大家关注谱度众合 (●’◡’●)

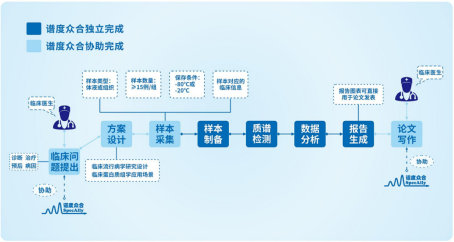
我司专业团队及临床蛋白质组学一站式服务